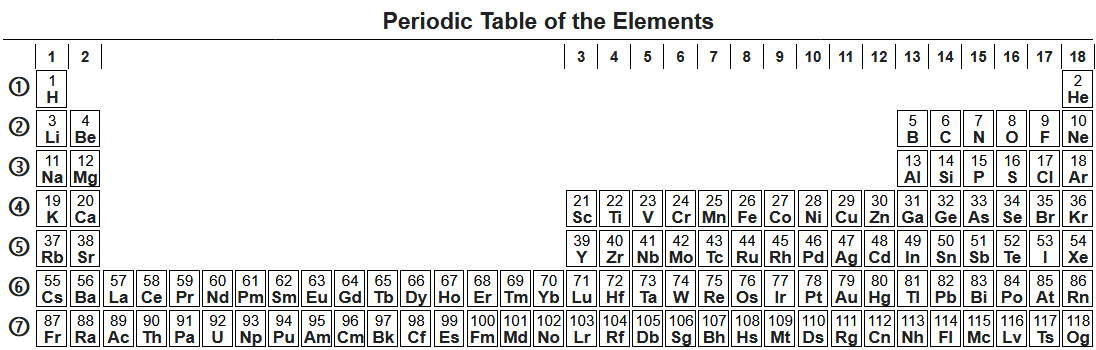
Периодический закон Менделеева является одним из фундаментальных законов химии, который формулирует основные принципы классификации и устройство таблицы химических элементов. Формулировка этого закона в современной науке основывается на идее, что химические элементы располагаются в периодической системе таким образом, чтобы их свойства варьировались периодически с увеличением атомного номера.
Устройство таблицы Менделеева представляет собой матрицу, в которой элементы располагаются по горизонтали в порядке возрастания атомного номера. Каждый элемент занимает одну ячейку в таблице, которая содержит информацию о его атомном номере, символе, относительной атомной массе и химических свойствах.
Основные принципы классификации химических элементов в таблице Менделеева основываются на их электронной структуре и химических свойствах. В основе этой классификации лежит идея периодичности химических свойств элементов на основе их электронной конфигурации. Каждый горизонтальный ряд таблицы называется периодом, а вертикальная группа — группой. Периоды и группы связаны с определенными электронными оболочками и подобными химическими свойствами.
Современная формулировка периодического закона Менделеева
Устройство таблицы Менделеева является регулярной и систематической. Она состоит из строк, называемых периодами, и столбцов, называемых группами. Каждый элемент представлен отдельной ячейкой, в которой указан его химический символ, атомный номер и относительная атомная масса. В центре таблицы расположены лантаноиды и актиноиды, которые вынесены в отдельные строки для компактности.
Основные принципы классификации химических элементов в таблице Менделеева включают:
- Группировку элементов, имеющих схожие свойства, в одну группу.
- Упорядочение элементов в порядке возрастания их атомных номеров.
- Разделение элементов на блоки в зависимости от наличия свободных электронов в электронной оболочке.
- Расположение элементов в порядке возрастания их атомных масс.
Классификация элементов в таблице Менделеева позволяет увидеть закономерности в их химическом поведении, определить группы элементов с схожими свойствами и предсказать свойства еще неизвестных элементов. Периодический закон Менделеева оказал огромное влияние на развитие химии и стал основой для современных представлений о взаимодействии химических элементов и структуре вещества.
Устройство таблицы Менделеева
Таблица Менделеева состоит из горизонтальных рядов, называемых периодами, и вертикальных столбцов, называемых группами.
Каждый элемент в таблице Менделеева представлен ячейкой, которая содержит следующую информацию:
- Атомный номер — количество протонов в ядре атома, которое также определяет порядковый номер элемента в таблице;
- Символ элемента — химический символ, используемый для обозначения элемента, например, H для водорода и O для кислорода;
- Относительная атомная масса — среднее значение массы атомов элемента, учитывающее их изотопы;
- Группа — номер вертикального столбца, который указывает на количество валентных электронов и химические свойства элемента;
- Период — номер горизонтального ряда, который указывает на количество электронных оболочек.
Помимо основных информационных элементов, таблица Менделеева также имеет дополнительные блоки, такие как лантаноиды и актиноиды, которые находятся в отдельных строках под основной таблицей. В этих блоках также указывается атомный номер и символ элемента.
Устройство таблицы Менделеева позволяет систематически организовать и классифицировать все известные химические элементы, а также предсказывать свойства и взаимодействия между ними. Это является фундаментальным инструментом для изучения и понимания химии и материи в целом.
| Атомный номер | Символ элемента | Относительная атомная масса | Группа | Период |
|---|---|---|---|---|
| 1 | H | 1.008 | 1 | 1 |
| 2 | He | 4.0026 | 18 | 1 |
| 3 | Li | 6.94 | 1 | 2 |
Исторический обзор:
Периодический закон был сформулирован русским химиком Дмитрием Ивановичем Менделеевым в 1869 году. Однако, сама мысль о существовании периодического закона возникла задолго до этого.
Первые попытки классификации химических элементов были предприняты в начале XIX века. Химик Йоган Бёерельс в 1817 году опубликовал свою таблицу, в которой элементы были разделены на три основные группы: металлы, неметаллы и оксиды.
Следующим шагом в развитии периодической системы элементов стало открытие таких элементов, как стронций, свинец и магний, которые не соответствовали ранее известным группам. Это стало основой для новых классификаций. Например, химики Жюль Гошлё и Альександр Мишель рассматривали элементы по группам по возрастанию атомных масс, а Йоганн Дёберейнер впервые предложил идею «трёхтелого закона», в котором элементы разделены на три группы с определенными характеристиками.
В 1869 году Дмитрий Менделеев представил свою таблицу, которая стала отправной точкой для современной периодической системы элементов. Он классифицировал элементы по возрастанию атомных масс, а также оставил места для открытия новых элементов.
В дальнейшем были открыты новые элементы, и периодическая система Менделеева продолжала развиваться. Также было обнаружено, что периодический закон можно описать с использованием атомных номеров элементов, а не только их атомных масс.
Сегодня периодическая таблица Менделеева является основой для изучения химии и представляет собой удобное и систематическое устройство всех известных химических элементов.
Логика расположения элементов:
Устройство таблицы Менделеева основывается на логике расположения химических элементов их свойств и химической активности. Каждый элемент имеет уникальное атомное число, которое указывает на количество протонов в ядре его атома. Таблица Менделеева располагает элементы в порядке возрастания атомного номера, начиная с элемента с наименьшим атомным номером.
Главная особенность таблицы Менделеева заключается в том, что она группирует элементы в периоды и группы. Периоды расположены горизонтально и указывают на количество энергетических уровней в атоме элемента. Группы располагаются вертикально и отражают химические свойства элементов. Всего существует 7 периодов и несколько групп, однако некоторые группы могут быть дополнительно разделены на подгруппы.
Каждый элемент таблицы Менделеева обозначается символом, который состоит из одной или двух букв. При этом, первая буква символа является заглавной, а вторая — строчной (например, H — водород, Fe — железо). Элементы схожих свойств располагаются в одной группе и образуют вертикальные столбцы. Периоды таблицы отражают повышение энергетического уровня электронной оболочки и заключают в себе разнообразие элементов с разными физическими и химическими свойствами.
Таким образом, логика расположения элементов в таблице Менделеева позволяет систематизировать все известные химические элементы и предоставляет наглядное представление о их свойствах и классификации.
Современная форма таблицы Менделеева:
В современной форме таблицы Менделеева элементы располагаются в 18 группах и 7 периодах. Группы вертикально разделены на блоки: s-блок, p-блок, d-блок и f-блок. Структура таблицы Менделеева позволяет удобно отображать основные свойства элементов и их химическую активность.
Горизонтальные строки таблицы Менделеева называются периодами, их количество соответствует основным энергетическим уровням атомов. Вертикальные столбцы называются группами и отражают общий характер химических свойств элементов в данной группе.
Каждый элемент таблицы Менделеева указывает на своем месте свой химический символ, атомный номер и относительную атомную массу. Также можно прочитать имя элемента и его химические свойства, такие как электроотрицательность, радиус атома, энергия ионизации и т.д.
Основные принципы классификации химических элементов
Классификация химических элементов основывается на периодическом законе Менделеева, который формулировался и развивался на протяжении многих лет. Сейчас таблица Менделеева представляет собой систематическое устройство, в котором элементы расположены по возрастанию атомных номеров и сгруппированы по химическим свойствам.
Основными принципами классификации химических элементов в таблице Менделеева являются:
- Периоды — горизонтальные ряды элементов. Каждый период начинается с нового уровня энергии электронов и имеет определенное количество электронных оболочек.
- Группы — вертикальные столбцы элементов. В каждой группе элементы имеют одинаковое количество электронов на внешней оболочке и, следовательно, обладают схожими химическими свойствами.
- Валентность — способность элемента соединяться с другими элементами и образовывать химические связи. Она определяется числом электронов на внешней оболочке элемента и является одним из ключевых факторов, влияющих на химические реакции и взаимодействия элементов.
- Металлы, полуметаллы и неметаллы — в зависимости от своих химических свойств, элементы в таблице Менделеева разделены на эти три основные группы. Металлы обладают хорошей электропроводностью и обычно имеют металлический блеск, полуметаллы проявляют свойства и металлов, и неметаллов, неметаллы же характеризуются плохой электропроводностью и различными другими свойствами.
Эти основные принципы классификации позволяют систематизировать и упорядочить большое количество химических элементов и делают таблицу Менделеева мощным инструментом для изучения и понимания химии.
Химические свойства:
Химические свойства элементов в таблице Менделеева представлены в виде их химической активности, электроотрицательности, атомного радиуса и других параметров.
Химическая активность элементов определяется их способностью образовывать химические соединения с другими элементами. Элементы, находящиеся в одной группе таблицы Менделеева, обладают схожими химическими свойствами, так как имеют одинаковое число электронов на внешнем энергетическом уровне.
Электроотрицательность элементов характеризует их способность притягивать электроны в химических соединениях. Элементы с высокой электроотрицательностью, такие как кислород и хлор, обладают большей способностью к образованию ионо- и ковалентных связей.
Атомный радиус элемента определяется размером его атома. Атомы элементов в таблице Менделеева увеличиваются в размере по мере движения слева направо и сверху вниз.
| Элемент | Химическая активность | Электроотрицательность | Атомный радиус |
|---|---|---|---|
| Литий | Высокая | 0,98 | 152 пм |
| Магний | Средняя | 1,31 | 160 пм |
| Кислород | Высокая | 3,44 | 60 пм |
В таблице приведены значения химической активности, электроотрицательности и атомного радиуса для некоторых элементов. Эти параметры являются ключевыми при описании химических свойств элементов в таблице Менделеева.
Вопрос-ответ:
Каково устройство таблицы Менделеева?
Таблица Менделеева состоит из строк, называемых периодами, и столбцов, называемых группами. Периоды расположены горизонтально, а группы — вертикально. Каждый элемент располагается на пересечении определенного периода и определенной группы. В таблице Менделеева элементы упорядочены в порядке возрастающего атомного номера.
Какие основные принципы классификации химических элементов используются в таблице Менделеева?
Основными принципами классификации химических элементов в таблице Менделеева являются атомный номер элемента, его атомная масса и химические свойства. Кроме того, элементы располагаются в таблице таким образом, чтобы элементы с похожими свойствами находились в одной вертикальной группе.
Какова современная формулировка периодического закона Менделеева?
Современная формулировка периодического закона Менделеева гласит, что свойства химических элементов периодически изменяются с увеличением их атомного номера. Это означает, что элементы, расположенные в одной вертикали в таблице Менделеева, имеют схожие химические свойства.
Какие элементы классифицированы в таблице Менделеева?
В таблице Менделеева классифицируются все известные элементы, включая искусственно созданные элементы. На данный момент известно 118 элементов. Каждый из них имеет свое уникальное место в таблице Менделеева в соответствии с его атомным номером и химическими свойствами.
Каким образом происходит расположение элементов в таблице Менделеева?
Расположение элементов в таблице Менделеева происходит в порядке возрастания атомного номера, начиная с самого легкого элемента — водорода. При этом элементы с похожими химическими свойствами ставятся в одну вертикальную группу. Это позволяет упорядочить элементы и облегчает их классификацию.
Какая современная формулировка периодического закона Менделеева?
Современная формулировка периодического закона Менделеева гласит, что свойства химических элементов периодически повторяются при возрастании их атомных номеров. Это означает, что элементы, находящиеся в одной группе (вертикальном ряду) таблицы Менделеева, имеют схожие химические свойства.